

近日🈳,張凡教授研究團隊構築了腫瘤微環境響應的近紅外二區稀土發光納米顆粒-染料Förster能量共振轉移(FRET)體系,利用近紅外二區熒光壽命成像手段對小鼠原位肝腫瘤進行了精準檢測,有望為活體深組織熒光成像檢測研究提供新的思路。相關研究論文“A Tumor-Microenvironment-Responsive Lanthanide-Cyanine FRET Sensor for NIR-II Luminescence-Lifetime In Situ Imaging of Hepatocellular Carcinoma”在線發表於《先進材料》(Advanced Materials)🦶🏻。張凡教授課題組的博士生趙夢瑤與已畢業博士生李本浩為論文共同第一作者🏊🏻♀️。
稀土摻雜近紅外二區下轉換納米顆粒作為成像造影劑,被廣泛應用於生物體熒光成像👊🏼、檢測等領域🎼。然而,在熒光信號穿透生物組織的過程中,會因組織吸收與散射發生不可避免的熒光信號強度衰減🤜🔍。這為熒光成像的定性、定量檢測帶來了極大困擾🏚🏄🏿♂️。同時👩🏽⚕️,靜脈註射的納米顆粒會大量被肝臟捕獲,造成極高的熒光強度背景信號,這進一步提高了肝臟相關腫瘤的檢測難度。
針對目前存在的問題👨💻,張凡教授團隊提出了基於熒光壽命成像手段對原位肝腫瘤進行精準檢測❤️。作者構築了以近紅外二區發光的釹摻雜稀土納米顆粒作為能量供體,針對腫瘤微環境中活性氮物種響應的染料MY-1057作為能量受體。探針的熒光壽命由表面MY-1057受體數量決定,並且在腫瘤微環境活性氮物種存在下熒光壽命發生線性恢復🚑。值得關註的是,與熒光強度恢復曲線不同,熒光壽命恢復曲線在不同模擬組織穿透深度下保持高度一致🧑🏿🏭。因此🧑🏽🦲,熒光壽命探針可對腫瘤微環境中活性氮物種進行定量檢測。相比於低信噪比的熒光強度成像,熒光壽命成像可準確地將肝臟腫瘤與正常肝組織區分開🙂↕️,其結果與臨床標準磁共振成像以及解剖結果高度吻合。這種基於熒光壽命成像的肝腫瘤原位檢測新技術可被廣泛推廣至其他活體內生物活性物質的定性📷、定量檢測🧑🏼。
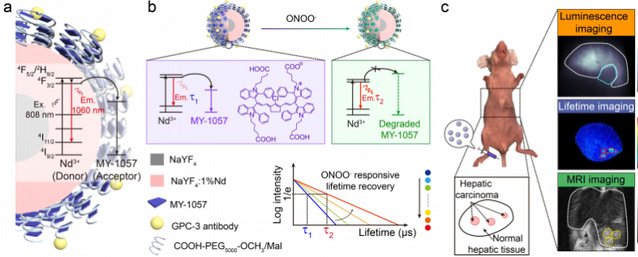
圖1. (a)熒光壽命探針結構示意圖👳🏿♀️。(b)熒光壽命探針響應腫瘤微環境中活性氮物種的壽命變化示意圖。(c)熒光壽命成像精準檢測原位肝腫瘤。
該工作得到了沐鸣开户𓀝、聚合物工程國家重點實驗室、沐鸣平台先進材料實驗室、國家重點研發項目、國家自然科學基金優秀青年基金、上海市科學技術委員會重點基礎研究項目的大力支持。
該論文作者為:Mengyao Zhao+, Benhao Li+, Yifan Wu, Haisheng He, Xinyan Zhu, Hongxin Zhang, Chaoran Dou, Lishuai Feng, Yong Fan, Fan Zhang*
全文鏈接: https://onlinelibrary.wiley.com/doi/full/10.1002/adma.202001172





